近日,哈尔滨医科大学“疾病基因及分子靶点创新研究”头雁团队的郑桐森-郝大鹏联合团队在肿瘤免疫治疗领域取得重要进展,研究论文《CD160 dictates anti-PD-1 immunotherapy resistance by regulating CD8+ T cell exhaustion in colorectal cancer》于9月9日在线发表(Nature Cell Biology,2025)。研究团队首次发现一种在回肠中特异富集的CD160+CD8+ T细胞亚群兼具强大的抗肿瘤细胞毒性与抗终末耗竭功能,并能有效克服PD-1单抗治疗耐药,为肠癌患者提供了全新治疗策略。

背景与挑战
近年来,以PD-1/L1单抗为代表的免疫治疗改变了肿瘤的治疗格局,但晚期肠癌、胆管癌及胰腺癌等肿瘤获益有限且容易耐药,严重影响治疗预后。针对这一重大临床医学难题,团队另辟蹊径,从“肿瘤发生的器官易感性差异”入手,围绕“同属消化道,位置相邻,解剖相似,大肠肿瘤高发,而小肠几乎不得癌症”这一百年医学谜题,整合哈尔滨医科大学遗传学、肿瘤学、生物信息学、外科学、内科学、病理学及药理学等领域的科研人员,深入挖掘这一差异背后的原因和机制,解析小肠独特的免疫微环境,寻找特异的基因及治疗靶点。
关键发现
1.单细胞测序揭示回肠、结肠及结肠肿瘤的免疫图谱差异
团队整合回肠、结肠、肿瘤等多部位组织进行单细胞RNA/TCR/BCR测序分析,绘制免疫细胞图谱,揭示了不同组织间免疫细胞分布的显著异质性。发现肿瘤转录特征与回肠类似的肠癌患者预后更优,其中T细胞是组织免疫微环境差异的核心因素。
2. CD160+CD8+ T细胞的组织特异性与抗终末耗竭潜能
首次发现CD160+CD8+T细胞亚群在肠道的分布具有组织特异性,在回肠中高度富集,而在结肠、肿瘤组织中逐渐降低。相较于CD160-亚群,CD160+亚群祖耗竭水平更高、终末耗竭水平更低,具有抗终末耗竭潜能,是维持抗肿瘤免疫应答的关键。
3. CD160通过结合PI3K(p85α)亚基提升T细胞效应功能并克服PD-1单抗耐药
CD160+CD8+ T细胞展现出更优越的细胞毒性和抗终末耗竭能力,可持续发挥抗肿瘤效应。临床相关性分析证实,肿瘤浸润CD8+ T细胞的CD160表达水平与PD-1单抗治疗应答率呈正相关。CD160+CD8+ T细胞输注既能协同增敏PD-1单抗疗效,还能克服PD-1单抗耐药。CD160可通过结合PI3K(p85α)亚基,激活AKT–NF-κB信号通路,上调FcεR1γ和4-1BB分子表达,提升CD8+ T细胞的效应功能。该研究不仅揭示了肠道组织特异性免疫调控新机制,也为跨器官免疫治疗策略提供了全新研究模式。
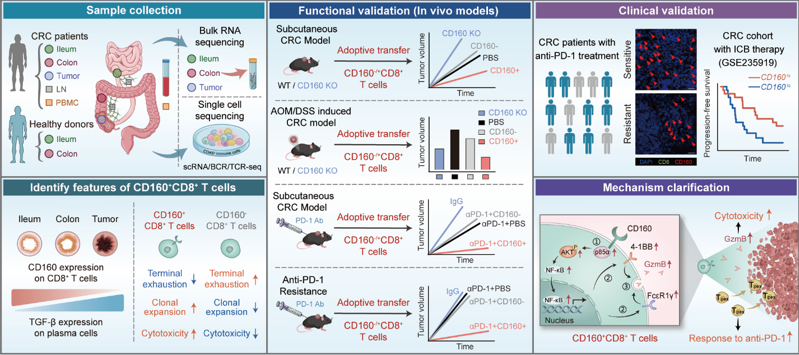
图1 “他山之石,可以攻玉”:小肠CD160+CD8+ T细胞的免疫优势,为大肠癌治疗提供跨器官借鉴
转化应用前景
项目研究成果已经获国家专利授权(CN 118161619 B)。相较于TIL、CAR-T等细胞疗法存在制备难、扩增差、费用高、不良反应明显等局限,CD160+CD8+ T细胞治疗产品基于患者外周血制备,具有工艺简单、自体细胞回输安全性高、易扩增、高效能等优势。团队目前已经发起一项前瞻性、开放、干预性IIT研究,旨在探索CD160+CD8+ T细胞联合PD-1单抗治疗肠癌的安全性与初步疗效,研究已进入国家干细胞专家委员会评审阶段,有望为更多免疫难治性肿瘤患者提供治疗新策略。
国际权威评述
杂志同期邀请了国际著名肿瘤免疫学专家Ping-Chih Ho教授为该项研究撰写评述,认为CD160+CD8+ T细胞与免疫检查点阻断疗法的联合将成为极具潜力的治疗策略,有望显著提升肠癌患者的临床疗效与预后。

研究团队
本研究在黑龙江省头雁行动计划支持下完成,哈尔滨医科大学为独立完成单位,附属肿瘤医院的郑桐森教授与基础医学院郝大鹏教授作为共同通讯作者。郑桐森教授致力于消化系统肿瘤的发病机制与临床综合治疗,负责本项目的整体设计与组织实施,郝大鹏教授作为哈医大引进的国家级海外青年人才,主持完成了本研究的单细胞数据分析与靶点挖掘工作。丁楚杰助理研究员、赖世辉博士、高扬博士在导师们的指导下完成CD160靶点的功能和机制验证工作。
“跳出肿瘤研究肿瘤”,从“小肠-结肠”的器官差异出发破解癌症免疫治疗难题,是哈医大青年研究团队“以临床需求为导向,以转化研究为目标”的实践探索。未来,团队将继续深耕肿瘤免疫治疗难点,以跨器官视角探索更多治疗可能,为提升肿瘤免疫治疗水平贡献哈医力量。
























