一、项目名称:精准医学中心荧光PCR检测试剂采购
二、项目编号:HYDFSZLYY-2019-024
三、采购内容及采购预算金额:
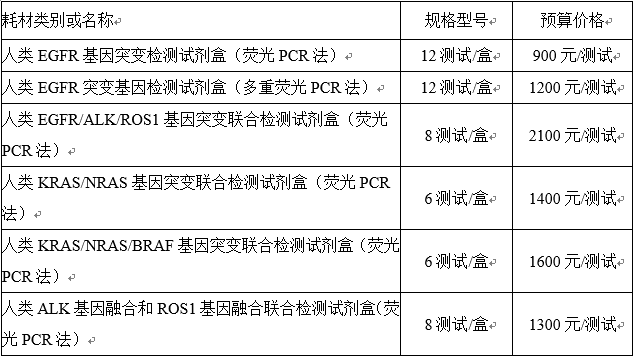
四、采购要求:详见附件1
五、申请理由:鉴于目前国内外指南专家共识对于非小细胞肺癌和肠癌患者,在进行靶向治疗之前必须常规检测EGFR,ALK,ROS1,KRAS,NRAS,BRAF基因的要求,为符合指南共识,满足临床需求,我科室预计开展相关检测项目。同时考虑到EGFR,ALK,ROS1,KRAS,
NRAS,BRAF单基因,多平台分别检测,浪费患者有限的样本量(特别是晚期患者穿刺活检组织体积小,组织量无法重复进行多次检测),延长出具报告时间及增加患者经济负担等因素,特申请使用EGFR/ALK/ROS1,KRAS/NRAS,KRAS/NRAS/BRAF,ALK/ROS1四种联合检测。
对于需要单检EGFR突变的患者使用EGFR基因突变检测试剂盒,并需要具备肠癌适应症,为满足伴随诊断患者在治疗中需要多次检测的治疗要求,将使用血液EGRF进行检测。所以我科室需购进一批厦门艾德生物医药科技股份有限公司生产的基因诊断试剂盒(如上表)。该公司生产厂的基因诊断试剂盒具有特异性强、灵敏度高、所需样本少、操作简单用时少等特点。EGFR基因突变检测试剂盒试剂盒具备肠癌适应症,EGFR突变基因检测试剂盒为血液检测,而多基因检测试剂盒能够满足更多的临床治疗需求,更加符合指南共识推荐。且全国多家省级三甲医院已使用,多项多中心大样本研究及临床多年使用结果验证符合临床需求。这次采购的试剂盒均获得国家药品监督管理局(NMPA)医疗器械注册证书,并由厦门艾德生物医药科技有限公司独家销售。
目前无具备以上合规的同类产品,因此申请单一来源采购。
六、专业人员姓名、工作单位、职称及论证意见:详见附件2
七、单一来源供应商:厦门艾德生物医药科技有限公司
供应商地址:厦门市海沧区鼎山路39号
八、公示期:2019年10月09日至2019年10月15日
如有其他潜在供应商对本项目采用单一来源方式采购有异议,请在公示期内将质疑书原件(含电子版)及法人代表授权书原件(含法人身份证复印件及授权委托人身份证复印件)送达采购人和采购代理机构。未在规定时间内送达的质疑为无效质疑。
采购人:黑龙江省肿瘤医院
地 址:哈尔滨市南岗区哈平路150号
联系人:孙先生
联系电话:0451-86298162
采购代理机构:中精信工程技术有限公司
地 址:哈尔滨市南岗区长江路189号四楼
项目经办人:姜盼 李志超
电 话:0451-87003479
电子邮箱:zjx87003479@163.com
2019年 10月08日
附件1:
1.人类EGFR基因突变检测试剂盒(荧光PCR法)的主要技术指标及技术参数
1.
试剂、配套及质控物质均有国家食品药品监督管理局认证的注册证。
2.
检测原理:采用扩增阻滞突变系统(ARMS)和荧光PCR技术,以样本DNA为检测对象,实现EGFR基因突变检测,适用于多种实时荧光定量PCR仪。
3.
试剂检测位点覆盖:检测EGFR基因18-21外显子上的≥21种突变。
4.
精密度:对EGFR精密度参考品重复检测10次,Ct值变异系数,CV值≤10%。
5.
灵敏度:试剂盒可检出 10 ngDNA 样品中含量低至 1%的 EGFR 基因突变。
6.
准确度:阳性和阴性参考品符合率均为100%。
7.
试剂质控:阴控、阳控、内控、外控四重质控降低假阴性和假阳性概率。
8.
适应症:肠癌
9.
性能评估:在发检测报告之前,供货商须为检测系统做性能验证,提供验证报告。
10.
试剂效期:试剂交付使用时,试剂效期大于180天。
11.
试剂稳定性:试剂效期内可长期 -20度储存。
12. 试剂特性:操作简便快捷、当天可出检测报告;适用标本类型有石蜡包埋组织样本和血浆样本。
2.人类EGFR突变基因检测试剂盒(多重荧光PCR法)的主要技术指标及技术参数
1.
试剂、配套及质控物质均有国家食品药品监督管理局认证的注册证。
2.
检测原理:采用扩增阻滞突变系统(ARMS)和荧光PCR技术,以血液样本cfDNA为检测对象,实现EGFR基因突变检测,适用于多种实时荧光定量PCR仪。
3.
试剂检测位点覆盖:检测EGFR基因18-21外显子上的≥30种突变。
4.
精密度:对EGFR精密度参考品重复检测10次,Ct值变异系数,CV值≤10%。
5.
灵敏度:试剂盒可检出 cfDNA 样品中含量低至 0.2%-0.8%的 EGFR 基因突变。
6.
准确度:阳性和阴性参考品符合率均为100%。
7.
试剂质控:阴控、阳控、内控、外控四重质控降低假阴性和假阳性概率。
8.
适应症:肺癌
9.
性能评估:在发检测报告之前,供货商须为检测系统做性能验证,提供验证报告。
10.
试剂效期:试剂交付使用时,试剂效期大于180天。
11.
试剂稳定性:试剂效期内可长期 -20度储存。
3.人类EGFR/ALK/ROS1基因突变联合检测试剂盒(荧光PCR法)的主要技术指标及技术参数
1.
试剂、配套及质控物质均有国家食品药品监督管理局认证的注册证。
2. 检测原理:采用扩增阻滞突变系统(ARMS技术),以样本DNA为检测对象,进行EGFR基因的突变检测,同时采用RT-PCR方法,以样本中的RNA为检测对象,实现ALK、ROS1融合基因的检测,适用于多种实时荧光定量PCR仪。
3. 试剂检测位点覆盖:检测样本中EGFR、ALK和ROS1基因的≥16种热点突变。
4. 精密度:对EAR精密度参考品重复检测10次,Ct值变异系数,CV值≤10%。
5. 灵敏度:试剂盒对7.5-15ng FFPE 样本中含有1%的EGFR基因突变,以及0.09-4.5ng
FFPE样本中含有450拷贝的ALK基因融合、ROS1基因融合装甲RNA均可准确检出。
6. 准确度:阳性和阴性参考品符合率均为100%。
7. 试剂质控:阴控、阳控、内控、外控四重质控,降低假阴性和假阳性概率。
8. 适应症:非小细胞肺癌
9. 性能评估:在发检测报告之前,供货商须为检测系统做性能验证,提供验证报告。
10. 试剂效期:试剂交付使用时,试剂效期大于180天。
11. 试剂稳定性:试剂效期内可长期 -20度储存。
4.人类KRAS/NRAS基因突变联合检测试剂盒(荧光PCR法)的主要技术指标及技术参数
1.
试剂、配套及质控物质均有国家食品药品监督管理局认证的注册证。
2.
检测原理:采用扩增阻滞突变系统(ARMS)和荧光PCR技术,以样本DNA为检测对象,实现KRAS/NRAS基因突变检测,适用于多种实时荧光定量PCR仪。
3.
试剂检测位点覆盖:KRAS基因第2、3、4外显子上≥12种体细胞热点突变、NRAS基因第2和3外显子上≥3种体细胞热点突变。
4.
精密度:对KRAS/NRAS精密度参考品重复检测10次,Ct值变异系数,CV值≤10%。
5.
灵敏度:试剂盒可检出 10 ngDNA 样品中含量低至1%的KRAS/NRAS基因突变。
6.
准确度:阳性和阴性参考品符合率均为100%。
7.
试剂质控:阴控、阳控、内控、外控四重质控,降低假阴性和假阳性概率。
8.
适应症:结直肠癌
9.
性能评估:在发检测报告之前,供货商须为检测系统做性能验证,提供验证报告。
10.
试剂效期:试剂交付使用时,试剂效期大于180天。
11.
试剂稳定性:试剂效期内可长期 -20度储存。
5.人类KRAS/NRAS/BRAF基因突变联合检测试剂盒(荧光PCR法)的主要技术指标及技术参数
1.
试剂、配套及质控物质均有国家食品药品监督管理局认证的注册证。
2.
检测原理:采用扩增阻滞突变系统(ARMS)和荧光PCR技术,以样本DNA为检测对象,实现KRAS/NRAS/BRAF基因突变检测,适用于多种实时荧光定量PCR仪。
3.
试剂检测位点覆盖:检测人类KRAS基因第2、3、4外显子上≥12种体细胞热点突变、人类NRAS基因第2和3外显子上≥3种体细胞热点突变和人类BRAF基因15号外显子的V600E热点突变。
4.
精密度:对KRAS/NRAS/BRAF精密度参考品重复检测10次,Ct值变异系数,CV值≤10%。
5.
灵敏度:试剂盒可检出 10 ngDNA 样品中含量低至1%的KRAS/NRAS/BRAF基因突变。
6.
准确度:阳性和阴性参考品符合率均为100%。
7.
试剂质控:阴控、阳控、内控、外控四重质控,降低假阴性和假阳性概率。
8.
适应症:结直肠癌
9.
性能评估:在发检测报告之前,供货商须为检测系统做性能验证,提供验证报告。
10.
试剂效期:试剂交付使用时,试剂效期大于180天。
11.
试剂稳定性:试剂效期内可长期 -20度储存。
6.人类ALK基因融合和ROS1基因融合联合检测试剂盒(荧光PCR法)的主要技术指标及技术参数
1.
试剂、配套及质控物质均有国家食品药品监督管理局认证的注册证。
2.
检测原理:采用RT-PCR方法,以样本中的RNA为检测对象,实现ALK、ROS1融合基因的检测,适用于多种实时荧光定量PCR仪。
3.
试剂检测位点覆盖:检测ALK基因和ROS1 基因的≥16种融合突变。
4.
精密度:对AR精密度参考品重复检测10次,Ct值变异系数,CV值≤10%。
5.
灵敏度:试剂盒对0.09-4.5ng FFPE样本中含有450拷贝的ALK基因融合、ROS1基因融合装甲RNA均可准确检出。
6.
准确度:阳性和阴性参考品符合率均为100%。
7.
试剂质控:阴控、阳控、内控、外控四重质控,降低假阴性和假阳性概率。
8.
适应症:非小细胞肺癌
9.
性能评估:在发检测报告之前,供货商须为检测系统做性能验证,提供验证报告。
10.
试剂效期:试剂交付使用时,试剂效期大于180天。
11. 试剂稳定性:试剂效期内可长期 -20度储存。
附件2:


























